Коагуляция частиц ускоряется при добавлении в коллоидную систему электролита. Минимальная концентрация электролита, вызывающая за определенный промежуток времени определенный видимый эффект коагуляции (изменение цвета, помутнение), называется порогом коагуляции или критической концентрацией. Эта величина служит сравнительным критерием агрегативной устойчивости дисперсной системы. Экспериментальное исследование процесса коагуляции электролитами привело к установлению эмпирического правила (правило Шульца-Гарди), согласно которому критическая концентрация иона-коагулятора уменьшается с увеличением его валентности: для двухвалентного иона порог коагуляции в десятки раз, а для трехвалентного – в сотни раз меньше, чем для одновалентного. Увеличение коагулирующего действия иона с повышением его валентности объясняется более сильным эффектом сжатия ДЭС ионами с большей валентностью.
Многовалентные ионы могут вызвать перезарядку поверхности; при коагуляции многовалентными ионами наблюдается чередование концентрационных зон устойчивого и неустойчивого состояния раствора — неправильные ряды.
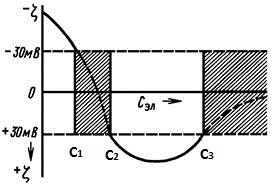
Явление неправильных рядов становится понятным, если вспомнить об изменении структуры ДЭС при перезарядке поверхности:
1) зона концентраций 0 — С1 — зона устойчивого состояния системы;
2) зона концентраций С1 — С2 — происходит сжатие ДЭС трехвалентными ионами, которые, адсорбируясь на отрицательно заряженной поверхности, вызывают ее нейтрализацию — наблюдается нейтрализационная коагуляция; старый ДЭС и новый ДЭС, возникший после перезарядки поверхности, не обеспечивают преобладания сил отталкивания частиц — дисперсная система коагулирует;
3) зона концентраций С2 — С3 — новый ДЭС, возникший на поверхности частиц после перезарядки, приобрел достаточную величину и обеспечивает агрегативную устойчивость частиц.
4) при концентрациях, превышающих Сз, система вновь становится неустойчивой: произошло сжатие нового ДЭС вследствие повышения концентрации ионов в растворе, одноименных с противоионами в новом ДЭС (т, е, анионами); здесь имеет место так называемая концентрационная коагуляция.
Явление неправильных рядов объясняется тем, что при малых количествах введенного электролита многовалентных ионов недостаточно, чтобы скоагулировать золь. При этой концентрации электролита ζ-потенциал частиц выше его критического значения. При несколько больших количествах электролита его ионы уже проявляют коагулирующее действие.
При еще несколько больших концентрациях многовалентные ионы перезаряжают коллоидные частицы и золь становится опять устойчивым. В этой зоне ζ-потенциал снова выше критического значения, но противоположен по знаку ζ-потенциалу частиц исходного золя. Наконец, при высоком содержании введенного электролита многовалентные иона снова и уже окончательно коагулируют золь по механизму концентрационной коагуляции.
Источники:
1.Неправильные ряды [Электронный ресурс] // Краткий курс коллоидной химии. Руцков А.П. Режим доступа: http://chem21.info/page/004133021019156144165100143049250043219035069199/ 2.Практикум по коллоидной химии: Учеб.пособие для хим.-технол. спец. вузов/ Баранова В. И., Бибик Е.Е., Кожевникова Н.М. с.114 3.Явление неправильных рядов.[Электронный ресурс] // Студопедия. Режим доступа: http://studopedia.ru/1_120749_osobie-yavleniya-nablyudayushchiesya-pri-koagulyatsii-elektrolitami.html